Briumvi vs Ocrevus vs Kesimpta: Comprendre les options de traitement de la SEP
Dernière mise à jour : 15 janvier 2024

Vous pouvez légalement accéder à de nouveaux médicaments, même s'ils ne sont pas approuvés dans votre pays.
Apprendre commentSi vous naviguez dans le paysage des traitements de la sclérose en plaques (SEP), Briumvi, Ocrevus et Kesimpta sont peut-être sur votre radar. Cet aperçu vous aidera à comprendre les principales similitudes et différences entre ces trois traitements importants de la sclérose en plaques.
Il couvre tous les aspects de ces produits, depuis leurs utilisations, leurs mécanismes d'action, leurs méthodes d'administration, leur efficacité, leurs effets secondaires, jusqu'à leurs coûts et leurs autorisations.
Brumvi vs Ocrevus vs Kesimpta: A quoi servent-ils ?
Similitudes
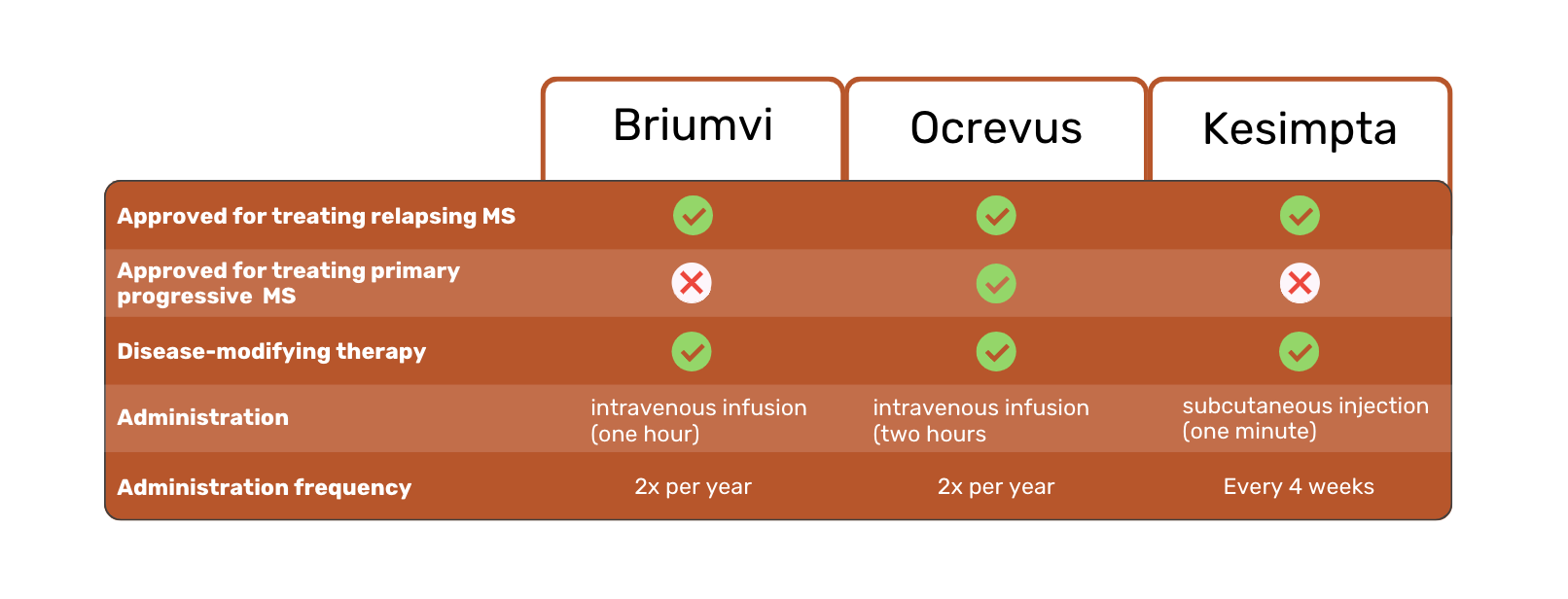
Ces trois thérapies sont prescrites pour le traitement de la sclérose en plaques (SEP). Plus précisément, la sclérose en plaques récurrente (SEP), y compris le syndrome cliniquement isolé, la SEP récurrente-rémittente et la SEP secondaire progressive active 1,2,3.
Différences
Ocrevus est le seul des trois médicaments à avoir reçu l'approbation de la FDA pour le traitement des patients atteints de sclérose en plaques primaire progressive (SEP-PP) 1.
Briumvi vs Ocrevus vs Kesimpta: Comment fonctionnent-ils ?
Briumvi, Ocrevus et Kesimpta sont tous des traitements de fond. En d'autres termes, ils visent à ralentir la progression de la SEP et à s'attaquer à sa cause sous-jacente, plutôt que de se concentrer uniquement sur ses symptômes.
Les trois médicaments sont des anticorps monoclonaux anti-CD20 et leur mécanisme d'action est globalement assez similaire. Leur mode d'action n'est pas totalement élucidé, mais les trois médicaments ciblent des cellules B spécifiques qui expriment la protéine CD20. On pense que ces cellules sont impliquées dans la progression de la SEP.
En s'attaquant à ces cellules B, Briumvi, Kesimpta et Ocrevus visent à réduire les taux de rechute de la SEP, à ralentir la progression de la maladie et à diminuer les lésions cérébrales actives chez les patients atteints de SEP 4.
Comment les sites Briumvi, Ocrevus et Kesimpta sont-ils administrés ?
Il existe des différences notables dans l'administration des trois thérapies.
Briumvi et Ocrevus sont disponibles sous forme de perfusion intraveineuse. Kesimpta est injecté dans la peau. Il s'agit d'une différence majeure, car elle permet aux patients de Kesimpta de s'auto-injecter à domicile, au lieu de recevoir une perfusion dans un hôpital ou une clinique.
Une autre différence entre les trois traitements de la SEP est la fréquence et la durée d'administration. Briumvi nécessite des perfusions d'une heure deux fois par an. En comparaison, Ocrevus nécessite deux perfusions de deux heures par an. Kesimpta doit être injecté toutes les quatre semaines.

Quelle est l'efficacité des sites Briumvi, Ocrevus et Kesimpta?
En termes d'efficacité, les trois médicaments ont montré des résultats similaires dans la réduction des rechutes et le ralentissement de la progression du RMS. Voici quelques points saillants des résultats de leurs essais cliniques.
Ocrevus résultats des essais cliniques
-
Résultats chez les patients atteints de RMS
Dans le cadre de deux essais cliniques menés sur une période de deux ans, le site Ocrevus a été comparé à un autre traitement autorisé contre la sclérose en plaques, Rebif.
Les résultats des études ont montré une réduction de 46 % des rechutes chez les patients sous Ocrevus , par rapport aux patients sous Rebif. 83 % des patients sous Ocrevus n'ont pas connu de rechute, contre 71 % des patients sous Rebif 4.
Au cours des deux années de l'étude, les personnes prenant Ocrevus avaient 40 % moins de risques de voir leur handicap progresser que celles prenant Rebif. En ce qui concerne les lésions T1 Gd+, les patients sous Ocrevus présentaient 94 % de lésions en moins que les patients sous Rebif. La réduction des lésions est considérée comme un élément important du ralentissement de la progression de la SEP 4.
-
Résultats chez les patients atteints de SEP-PP
Pour évaluer sa sécurité et son efficacité chez les patients atteints de SEP-PP, le site Ocrevus a été comparé à un placebo.
Les résultats de l'étude clinique ont montré que 32,9 % des patients sous Ocrevus ont connu une progression de leur handicap, contre 39,3 % des patients sous placebo.
Les patients sous placebo ont vu le volume de leurs lésions T2 augmenter de 7 %, tandis que les patients sousOcrevus ont vu le volume de leurs lésions T2 diminuer de 3 %.
Résultats de l'essai clinique Briumvi
L'efficacité et la sécurité de Briumvi ont été testées dans deux essais cliniques contre un autre traitement de la sclérose en plaques, le tériflunomide.
Les résultats des essais cliniques ont montré que les patients sous Brumvi ont connu 49 % (essai 1) et 59 % (essai 2) de rechutes en moins que les patients sous tériflunomide. Parmi les personnes prenant Briumvi, 86 % (essai 1) et 87 % (essai 2) n'ont pas eu de rechute, contre 74 % (étude 1) et 72 % (étude 2) des patients sous tériflunomide.
Les patients atteints de Briumvi présentaient 97 % (essais 1 et 2) de lésions T1 Gd+ en moins que les patients atteints de tériflunomide.
Kesimpta résultats des essais cliniques
Comme Briumvi, Kesimpta a été testé contre le tériflunomide dans deux essais cliniques.
Les résultats ont montré une diminution de 51% (essai 1) et de 58% (essai 2) des rechutes chez les patients du site Kesimpta par rapport aux patients du site tériflunomide.
La progression du handicap après l'apparition des symptômes était 34% (3 mois après l'apparition des symptômes) et 33% (6 mois après l'apparition des symptômes) moins probable pour les patients du site Kesimpta que pour les patients du tériflunomide.
Kesimpta ont présenté 98 % (essai 1) et 94 % (essai 2) de lésions T1 Gd+ en moins par rapport aux patients sous tériflunomide. Les patients sous Kesimpta ont également présenté 82 % (essai 1) et 85 % (essai 2) de lésions T2 en moins.


Briumvi vs Ocrevus vs Kesimpta: Sécurité et effets secondaires
Selon leurs informations de prescription, les effets secondaires les plus courants associés aux traitements Briumvi, Ocrevus et Kesimpta sont pour la plupart similaires. Une vue d'ensemble, avec quelques nuances, est présentée ci-dessous.
Briumvi effets secondaires
- Réactions à la perfusion, y compris fièvre, frissons, maux de tête, symptômes pseudo-grippaux 5.
- Infections. Le taux global d'infections était de 56 %, dont 5 % étaient considérées comme graves. Les infections les plus fréquemment signalées étaient celles des voies respiratoires supérieures et des voies urinaires 5.
Ocrevus les effets secondaires
- Réactions à la perfusion, notamment démangeaisons cutanées, éruptions cutanées, difficultés respiratoires, gonflement et douleur de la gorge, hypotension, fièvre, fatigue 6.
- Infections. Le taux global d'infections était de 58%. Les infections les plus fréquemment signalées étaient celles des voies respiratoires supérieures et inférieures, ainsi que les infections cutanées et les infections liées à l'herpès 6.
Kesimpta les effets secondaires
- Réactions liées à l'injection, notamment gonflement, démangeaisons et douleur 7.
- Infections. Le taux global d'infections était de 51,26 % à 52,7 %, dont 1,8 % à 2,5 % étaient considérées comme graves. Les infections les plus fréquemment signalées étaient celles des voies respiratoires supérieures et des voies urinaires 7.
- Maux de tête.
Briumvi, Kesimpta ou Ocrevus entraînent-ils une leucoencéphalopathie multifocale progressive (LMP) ?
La LEMP est une infection virale rare du cerveau, généralement observée chez les personnes immunodéprimées. Quelques cas de LEMP ont été rapportés après un traitement par Ocrevus 6.
Bien qu'aucun cas de LEMP n'ait été signalé après un traitement par Briumvi ou Kesimpta , il est important de garder à l'esprit que la LEMP peut survenir après un traitement par l'une de ces thérapies.
Briumvi vs Ocrevus vs Kesimpta: Comparaison des prix
Lorsqu'il s'agit de médicaments qui ne sont pas encore largement disponibles, les coûts ont tendance à varier en fonction de votre lieu de résidence, de vos fournisseurs ou de votre couverture d'assurance.
Vous trouverez ci-dessous une approximation des coûts annuels de traitement avec Briumvi, Ocrevus, et Kesimpta, en supposant qu'il n'y ait pas de couverture d'assurance.
Combien coûte Briumvi sans assurance ?
Pour les patients des Etats-Unis, où Briumvi est approuvé et disponible sur le marché, le coût annuel du traitement est estimé à 59 000 USD. Cette somme couvre 2 perfusions de 450 mg (6 flacons au total). À ce prix, Briumvi est le traitement contre la sclérose en plaques le plus abordable aux États-Unis à l'heure actuelle 13.
Toutefois, la situation est différente pour les patients de l'UE et d'autres régions en dehors des États-Unis. Bien que le Brumvi soit autorisé dans l'UE, il n'y est pas encore disponible commercialement, ce qui entraîne des coûts d'approvisionnement plus élevés. Dès que le prix du Briumvi sera fixé dans l'UE et que le traitement sera disponible localement, il est probable que le prix pour les patients non américains baissera également. Nous avons observé une tendance similaire avec Kesimpta et Ocrevus, qui sont sur le marché européen depuis plusieurs années.
Entre-temps, une dose unique de 150 mg (6 ml) de Briumvi en dehors des États-Unis coûte environ 15 130 euros. Cela se traduit par un coût de traitement annuel d'environ 90 780 euros (6 flacons).
Combien coûte Kesimpta sans assurance ?
Une dose unique de 20 mg (0,4 ml) de Kesimpta coûte environ 1 700 euros.
Le traitement commence généralement par une dose initiale de 20 mg (0,4 ml), répétée une semaine et deux semaines plus tard. Les injections suivantes sont effectuées une fois par mois.
Cela signifie que vos frais de traitement annuels s'élèveront à environ 25.500 euros la première année, puis à environ 20.400 euros par la suite.
Combien coûte Ocrevus sans assurance ?
Une dose unique de Ocrevus (300 mg/mL) coûte environ 8 016 euros.
Le traitement commence généralement par une dose initiale de 300 mg, répétée deux semaines plus tard. Les perfusions suivantes sont effectuées une fois tous les 6 mois, à la dose recommandée de 600 mg.
Les coûts de traitement s'élèvent à environ 48 096 euros la première année et à 32 064 euros par la suite.


Où sont approuvés Briumvi, Ocrevus et Kesimpta ?
Briumvi et Kesimpta ne sont actuellement autorisés qu'aux États-Unis et dans l'UE 8, 9, 10, 11. Ocrevus est actuellement autorisé dans plus de 98 pays, dont les États-Unis, l'UE, le Canada, l'Australie et la Nouvelle-Zélande 12.
Briumvi, Ocrevus ou Kesimpta n'est pas (encore) approuvé ou disponible dans votre pays ? Si vous et votre médecin pensez que ces traitements pourraient vous être bénéfiques, prenez contact avec notre équipe d'experts en accès médical. Nous pourrons vous donner un devis personnalisé pour l'obtention de ces médicaments.
Références :
- OCREVUS® (ocrelizumab) | Traitement de la sclérose en plaques (SEP). Ocrevus, consulté le 22 août 2023.
- Traitement de la SEP récurrente I KESIMPTA® (ofatumumab). Kesimpta, consulté le 22 août 2023.
- BRIUMVI ® (ublituximab-xiiy). Briumvi, consulté le 22 août 2023.
- Résultats d'OCREVUS® (ocrelizumab) pour la SEP récurrente. Ocrevus, consulté le 22 août 2023.
- ID de référence : 5101565. TG Therapeutics, consulté le 22 août 2023.
- POINTS FORTS DES INFORMATIONS DE PRESCRIPTION. Genentech, consulté le 22 août 2023.
- POINTS FORTS DES INFORMATIONS DE PRESCRIPTION. Novartis, consulté le 22 août 2023.
- Briumvi | Agence européenne des médicaments. Agence européenne des médicaments, 13 juillet 2023.
- Approbation de BRIUMVI™ (ublituximab-xiiy) | TG Therapeutics, Inc. TG Therapeutics, 28 décembre 2022.
- La FDA approuve Kesimpta® (Ofatumumab), la première thérapie à base de cellules B auto-administrée pour les formes récurrentes de la SEP | MSAA. Multiple Sclerosis Association of America, 25 août 2020.
- Kesimpta |Agence européenne des médicaments. Agence européenne des médicaments, 29 janvier 2021.
- Ocrevus. Roche, consulté le 22 août 2023.
- La FDA approuve Briumvi (ublituximab-xiiy) pour la SEP récurrente. National MS Society, 28 décembre 2022.