Médicaments nouvellement approuvés pour la mucoviscidose
Dernière mise à jour : 16 novembre 2020
Vous pouvez légalement accéder à de nouveaux médicaments, même s'ils ne sont pas approuvés dans votre pays.
Apprendre commentLa mucoviscidose est une maladie génétique rare, potentiellement mortelle, qui touche plus de 70 000 personnes dans le monde. Elle est due à une mutation du gène CFTR, qui régule le transport du sel et de l'eau dans l'organisme. La mutation du gène CFTR laisse entrer trop de sel et d'eau dans les cellules. Il en résulte une accumulation de mucus épais et collant dans les tubes et les voies de passage de l'organisme. Ces blocages endommagent les poumons, le système digestif et d'autres organes. Les symptômes apparaissent dès la petite enfance et comprennent une toux persistante, des infections thoraciques et pulmonaires récurrentes et une faible prise de poids.
Il existe aujourd'hui plusieurs traitements qui contribuent à la prise en charge de la mucoviscidose. Le dernier médicament approuvé pour la mucoviscidose par l'Agence médicale européenne (EMA) est Kaftrio (elexacaftor/tezacaftor/ivacaftor).
L'approbation de Kaftrio (elexacaftor/tezacaftor/ivacaftor) par l'EMA en août 2020 intervient après l'approbation de Trikafta (elexacaftor/tezacaftor/ivacaftor; ivacaftor) en octobre 2019.
Voici un aperçu de chaque médicament pour vous aider, vous et votre médecin, à prendre une décision concernant le traitement de la mucoviscidose :
Trikafta elexacaftor/tezacaftor/ivacaftor; ivacaftor)
Le 21 octobre 2019, Trikafta elexacaftor/tezacaftor/ivacaftor; ivacaftor) a été approuvé par la Food and Drug Administration (FDA), États-Unis, pour le traitement des personnes âgées de plus de 12 ans atteintes de certaines formes de fibrose kystique (FK).
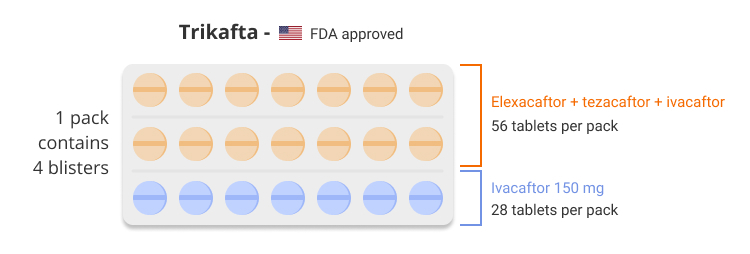
Trikafta (elexacaftor/tezacaftor/ivacaftor; ivacaftor) est une association d'ivacaftor, de tezacaftor et d'elexacaftor indiquée pour le traitement de la fibrose kystique (FK) chez les patients âgés de 12 ans et plus qui présentent au moins une mutation F508del dans le gène du régulateur de la conductance transmembranaire de la fibrose kystique (CFTR). Il est disponible sous forme de comprimés combinés à dose fixe co-packagés contenant 100 mg d'elexacaftor, 50 mg de tezacaftor et 75 mg d'ivacaftor, et de comprimés contenant 150 mg d'ivacaftor.
Kaftrio (elexacaftor/tezacaftor/ivacaftor)
Le 21 août 2020, Kaftrio (elexacaftor/tezacaftor/ivacaftor) a reçu une autorisation de mise sur le marché de l'EMA valable dans toute l'UE pour une utilisation en association avec Kalydeco (ivacaftor) afin de traiter les personnes âgées de plus de 12 ans atteintes de certaines formes de fibrose kystique (FK).
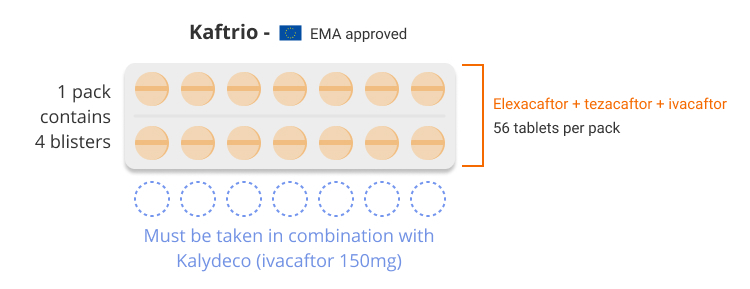
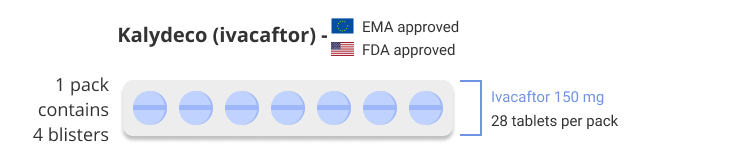
Kaftrio (elexacaftor/tezacaftor/ivacaftor) est indiqué dans un schéma d'association avec des comprimés d'ivacaftor 150 mg (non inclus dans l'emballage) pour le traitement de la fibrose kystique (FK) chez les patients âgés de 12 ans et plus qui présentent au moins une mutation F508del dans le gène du régulateur de la conductance transmembranaire de la fibrose kystique (CFTR). Il est disponible sous forme de comprimés combinés à dose fixe contenant 100 mg d'elexacaftor, 50 mg de tezacaftor et 75 mg d'ivacaftor.
Vous pouvez télécharger l'infographie complète sur les médicaments ici.
Si vous ou une personne de votre entourage souhaitez accéder à Trikafta elexacaftor/tezacaftor/ivacaftor; ivacaftor) ou à Kaftrio (elexacaftor/tezacaftor/ivacaftor) en association avec Kalydeco, nous pouvons vous aider.
Contactez notre équipe d'assistance aux patients pour plus d'informations.




