Adakveo vs Oxbryta: Connaître les alternatives au crizanlizumab
Dernière mise à jour : 15 janvier 2024
Vous pouvez légalement accéder à de nouveaux médicaments, même s'ils ne sont pas approuvés dans votre pays.
Apprendre comment
Suite au retrait de l'autorisation d'Adakveo crizanlizumab) dans l'UE, de nombreux patients et médecins doivent trouver une alternative à Adakveo .
Si vous avez bien répondu à votre traitement, vous pouvez toujours avoir accès à Adakveo même s'il n'est plus approuvé dans l'UE. Toutefois, si votre médecin préfère modifier votre traitement, il est bon de comprendre ce que cela signifie pour vous en tant que patient.
Dans cet article, nous allons nous pencher sur l'une des alternatives possibles à l'Adakveo dont votre médecin pourrait vous parler : Oxbryta voxelotor). Vous trouverez ici un aperçu rapide des similitudes et des différences entre Adakveo et Oxbryta.
Adakveo vs Oxbryta: A quoi servent-ils ?
Adakveo et Oxbryta sont tous deux des médicaments délivrés sur ordonnance et indiqués pour le traitement de la drépanocytose 1,2. Cependant, chacun de ces médicaments cible un aspect différent de la maladie.
L'Adakveo vise à réduire la fréquence des crises vaso-occlusives douloureuses, tandis que l'Oxbryta est utilisé pour traiter l'anémie hémolytique chez les patients drépanocytaires 1,2.
Pour quel âge Oxbryta est-il autorisé dans l'Union européenne ?
Contrairement à Adakveo, qui ne peut être utilisé que chez les patients âgés de 16 ans et plus, Oxbryta est également indiqué pour les patients pédiatriques.
Aux États-Unis, Oxbryta peut être prescrit à partir de l'âge de 4 ans, alors que dans l'UE, l'utilisation pédiatrique n'est approuvée qu'à partir de l'âge de 12 ans 1,2.
Crizanlizumab vs Voxelotor: Comment fonctionnent-ils ?
Si les deux médicaments visent à réduire les complications de la drépanocytose, ils s'attaquent à des aspects différents de la maladie.
Adakveo et la réduction des crises douloureuses
Adakveo vise à réduire la fréquence des crises douloureuses, qui surviennent lorsque des cellules sanguines malformées se bloquent dans les vaisseaux sanguins.
Le principe actif du médicament, le crizanlizumab, est un type spécifique de protéine connu sous le nom d'anticorps monoclonal. Cette protéine est formulée pour se lier à la sélectine P, une substance présente sur la couche externe des cellules qui tapissent les vaisseaux sanguins.
La P-sélectine aide les cellules à adhérer aux vaisseaux sanguins et est impliquée dans l'obstruction des vaisseaux lors des épisodes douloureux de la drépanocytose. En se connectant à la P-sélectine et en inhibant sa fonction, Adakveo vise à prévenir ces épisodes douloureux 3.
Oxbryta et la prévention de l'anémie
Oxbryta, quant à lui, vise à prévenir l'anémie associée à la drépanocytose.
Le principe actif d'Oxbryta, le voxelotor, augmente la capacité de l'hémoglobine à retenir l'oxygène et l'empêche de former des chaînes rigides dans les vaisseaux sanguins. Les globules rouges conservent ainsi leur forme et leur souplesse normales. Il réduit également le taux de leur destruction prématurée et prolonge leur durée de vie 4.
Quelle est l'efficacité d'Adakveo et d'Oxbryta?
L'efficacité d'Adakveo crizanlizumab et d'Oxbryta voxelotor) a été étudiée dans le cadre d'essais cliniques.
-
Résultats de l'essai clinique d'Adakveo
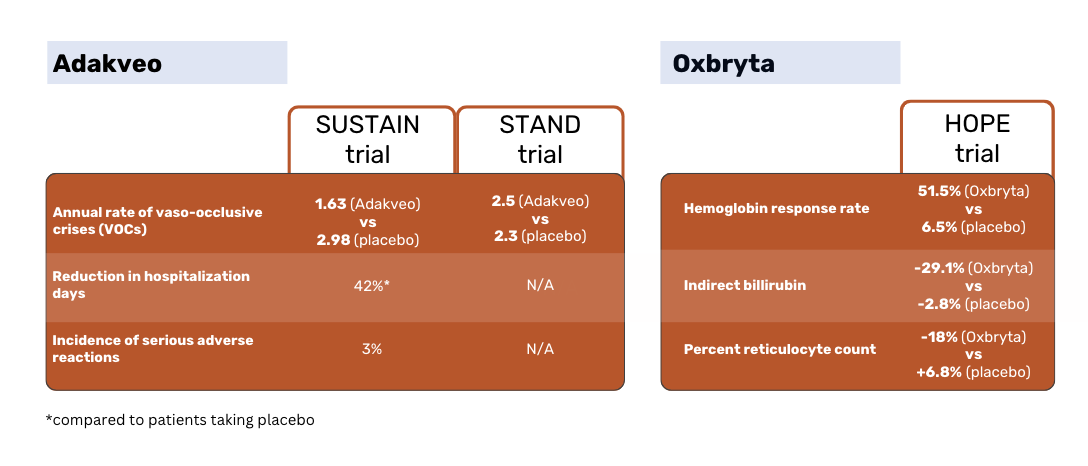
L'approbation de l'Adakveo par la FDA, ainsi que son autorisation initiale de mise sur le marché dans l'UE, étaient basées sur les résultats de l'étude clinique SUSTAIN. Cette étude comparait Adakveo (avec ou sans hydoxyurée) à un placebo.
Selon les résultats de l'étude SUSTAIN, les patients traités par Adakveo ont présenté un taux annuel médian de crises vaso-occlusives (COV) inférieur et statistiquement significatif - 1,63 contre 2,98 pour les patients sous placebo. 36 % des patients traités par Adakveo n'ont eu aucune crise vaso-occlusive au cours des 52 semaines de l'étude, contre 17 % des patients sous placebo 1.
Quels ont été les résultats du procès Adakveo STAND ?
L'étude globale de phase 3 STAND, qui comparait à nouveau Adakveo à un placebo, n'a pas réussi à démontrer une différence statistiquement significative dans le taux de COV entre les groupes de patients. Les patients traités par Adakveo ont eu en moyenne 2,5 crises douloureuses au cours de l'année de traitement - ce qui n'est pas significativement différent des 2,3 crises en moyenne rapportées dans le groupe placebo 3.
Les résultats peu convaincants de l'essai STAND ont servi de base à la révocation d'Adakveo dans l'UE.
-
Résultats des essais cliniques de l'Oxbryta
Dans l'essai HOPE, Oxbryta a été comparé à un placebo. L'efficacité était basée sur les taux de réponse de l'hémoglobine (Hb) définis comme une augmentation de l'Hb de >1 g/dL entre le début de l'étude et la semaine 24.
Les patients sous Oxbryta ont eu un taux de réponse de 51,1 % contre 6,5 % pour les patients sous placebo. La bilirubine indirecte a diminué de 29,1 % chez les patients sous Oxbryta , comparativement à une diminution de 2,8 % chez les patients sous placebo. Le pourcentage de réticulocytes a diminué de 18 % chez les patients sous Oxbryta et a augmenté de 6,8& chez les patients sous placebo 2.
Comme le montrent les données partagées, il n'est pas possible de faire une comparaison directe entre les deux médicaments, car des critères d'efficacité différents ont été utilisés dans leurs essais cliniques. Comme les deux traitements abordent la drépanocytose de manière différente, il est probable qu'Oxbryta ne remplacera pas directement Adakveo, mais fera plutôt partie d'un nouveau plan de traitement que votre médecin établira pour vous.

Adakveo vs Oxbryta: Sécurité et effets secondaires
Selon les informations de prescription, voici les effets secondaires les plus courants d'Adakveo et d'Oxbryta:
Effets secondaires d'Adakveo
- Nausées
- Douleurs articulaires
- Mal de dos
- Douleurs d'estomac
- Fièvre1.
Au cours de l'essai SUSTAIN, 3 % des patients ont présenté des réactions liées à la perfusion, caractérisées par des symptômes tels que maux de tête, frissons, vomissements, diarrhée, essoufflement ou respiration sifflante 1.
Oxbryta effets secondaires
- Maux de tête
- Diarrhée
- Douleurs d'estomac
- Nausées
- Éruption
- Fièvre 2.
Moins de 1 % des patients ayant participé aux essais cliniques ont présenté des réactions d'hypersensibilité graves, notamment des éruptions cutanées, un léger essoufflement, un léger gonflement du visage et une éosinophilie (augmentation du nombre de globules blancs)2.
Adakveo vs Oxbryta: Comparaison des prix
Les prix des médicaments qui ne sont pas encore approuvés ou disponibles ne sont donnés qu'à titre indicatif. Le prix final peut varier en fonction de votre lieu de résidence ou du fournisseur.
Coûts d'Adakveo par an
La dose recommandée pour Adakveo est de 5 mg/kg de masse corporelle toutes les 4 semaines. Cela signifie 13 perfusions par an. Pour une personne pesant 60 kg, il faut donc 13 perfusions x 300 mg d'Adakveo, soit 39 flacons du médicament.
Au prix d'environ 5 214 euros par flacon de 100 mg, le coût annuel d'un traitement par Adakveo s'élève à environ 203 346 euros 5.
Coûts annuels de l'Oxbryta
La posologie recommandée d'Oxbryta pour les patients dont le poids corporel est supérieur à 40 kg est de 1 500 mg d'Oxbryta une fois par jour, soit 3 comprimés de 500 mg chacun.
Une boîte de 90 comprimés de 500 mg coûte environ 40 365 euros et suffit pour un mois, sur la base de la posologie recommandée ci-dessus. Le coût annuel du traitement par Oxbryta s'élève donc à 484 380 euros 6.
Où Adakveo et Oxbryta sont-ils approuvés ?
Adakveo crizanlizumab) est actuellement autorisé dans plusieurs pays, dont les États-Unis, le Canada et l'Australie 7,9,10. Son autorisation de mise sur le marché conditionnelle dans l'UE a été révoquée en mai 2023 3.
Oxbryta voxelotor) est autorisé aux États-Unis, dans l'Union européenne et au Canada 4,8,9. Cependant, au sein de l'UE, Oxbryta n'est pas encore largement disponible sur le marché, car le délai entre l'autorisation et la mise sur le marché peut varier considérablement d'un pays à l'autre.
Adakveo ou Oxbryta n'est pas (plus) approuvé ou disponible dans votre pays ? Si vous et votre médecin pensez que ces traitements pourraient vous être bénéfiques, prenez contact avec notre équipe d'experts en accès aux médicaments. Nous pourrons vous donner une offre de prix personnalisée pour l'approvisionnement de ces médicaments.
Références :
- POINTS FORTS DES INFORMATIONS DE PRESCRIPTION. Novartis, consulté le 27 septembre 2023.
- POINTS FORTS DE L'INFORMATION SUR LA PRESCRIPTION. Oxbryta, consulté le 27 septembre 2023.
- Adakveo | Agence européenne des médicaments. Agence européenne des médicaments, consulté le 27 septembre 2023.
- Oxbryta | Agence européenne des médicaments. Agence européenne des médicaments, consulté le 27 septembre 2023.
- Acheter Adakveo (crizanlizumab) en ligne. Everyone.org, consulté le 27 septembre 2023.
- Acheter Oxbryta (voxelotor) en ligne. Everyone.org, consulté le 27 septembre 2023.
- Adakveo. Therapeutic Goods Administration (TGA), consulté le 27 septembre 2023.
- La FDA approuve un médicament pour traiter la drépanocytose chez les enfants. FDA, 17 décembre 2021.
- Nouveaux médicaments approuvés en 2019 - Meds Entry Watch. Canada.ca, 10 février 2021.
- La FDA approuve la première thérapie ciblée pour traiter les patients atteints d'une complication douloureuse de la drépanocytose. FDA, 15 novembre 2019.